1.2018年のGoogleの研究成果を振り返って(5/6)まとめ
・Googleの2018年のAI関連の研究や成果の振り返り
・ロボティクス、AIの他の分野への応用、ヘルスケア関連
・研究開発の結果から実際の製品として世に出たものまで幅広く紹介
2.2018年のGoogleの研究成果のまとめ
以下、ai.googleblog.comより「Looking Back at Google’s Research Efforts in 2018」の意訳です。久々のJeff Deanによる投稿です。
ロボティクス
2018年、私たちは、ロボットに現実世界で行動する方法を理解させると言う目標に対して大きな節目を達成しました。すなわち、ロボットに今まで見た事がない新しい物体を掴む事を学習させる事に成功したのです。(CoRL’18でベストペーパー賞を受賞しています)それも、人間が教える事なしに自律的に学習させたのです。
また、機械学習とサンプリングベースの手法(ICRA’18のサービスロボティクス部門でベストペーパー賞)を組み合わせることで、ロボットに動きを学習させる事や、より迅速なプランニングのためにロボットに位置を学習させる手法についても進歩しました。実物のロボットを使ってオンラインでディープ強化学習モデルを訓練することに成功し、ロボットの制御を安定させる、理論的に根拠のある新しい方法を見つけています。

AIの他分野への応用
2018年に、私たちは物理学と生物学のさまざまな問題に機械学習を適用しました。機械学習を使用すると、何百、何千というリサーチアシスタントがデータを掘り下げることに相当するものを科学者に提供することができ、それによって科学者はより創造的で生産的になることができます。
学術誌Nature Methodsに投稿した論文「high-precision automated reconstruction of neurons」では、これまでのディープラーニング手法に比べて、コネクトミクスデータの自動判読の精度を1桁向上させる新しいモデルを提案しました。

私達のアルゴリズムが鳴いている鳥の神経突起を辿っている様子
科学分野でMLを有効活用したいくつかの例には、次のものがあります。
・星の輝きを記録した膨大なデータから太陽系外の新しい惑星の発見
・短いDNA塩基配列の素性もしくは機能の検出
・焦点の合っていない顕微鏡画像の自動検出
・異なった手法で撮影された複数の色の細胞画像からデジタル画像を作成
・多数の分光器をペプチド鎖へ自動マッピング

事前に訓練されたTensorFlowモデルは、細胞の顕微鏡画像の焦点品質を評価します。境界線の色相と明るさは、それぞれ予測されるフォーカス品質と予測の不確かさを表します。
ヘルスケア
過去数年間、私たちは医療分野に対して機械学習を適用してきました。これは私たち一人ひとりが影響を受ける分野であり、機械学習が医療専門家の直感と経験を強化する事によってが大きな変化をもたらされると信じている分野です。
この分野での私たちの一般的なアプローチは、基本的な研究問題に取り組むためにヘルスケア組織と協力(臨床専門家からのフィードバックを使って結果をより堅牢にする)することと、その結果を権威があり、厳密に査読される科学および臨床ジャーナルに投稿する事です。
研究が臨床的および科学的に検証されたら、次にユーザーおよび仮想インフラ環境にて調査を行い、これを実際の臨床現場でどのように展開できるかを確かめます。2018年、私たちはコンピューター支援診断から臨床課題予測へと研究の成果を広げました。
2016年の終わりに、我々は糖尿病性網膜症の徴候について網膜眼底画像を評価するために訓練されたモデルがこのタスクで米国の医療委員会認定眼科医よりもわずかに上回って実行できることを示す研究を遡及研究で発表した。
2018年、網膜専門家によってラベル付けされた訓練用画像と専門家による判定(複数の網膜専門家が集まって各眼底画像に対して同一評価をくだす事で判定)を用いることによって、私達のモデルが網膜専門医と同等のレベルに到達した事を示す事ができました。
後に、私たちは、眼科医がこのMLモデルと協同する事により、眼科医単独の診断やMLモデル単独の予測より、正確な診断を下せる事ができるという研究結果を発表しました。私達は、この糖尿病性網膜症検出システムを、Googleの関連会社であるアルファの同僚と協力して、インドのアラビンド眼科病院とタイの保健省と提携しているラジャビティ病院を含む10カ所以上の施設で展開しました。
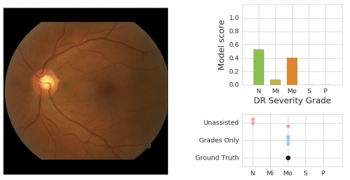
左側には、眼科医の判断パネルによって中等度のDR(Mo)と等級付けされた網膜眼底像がある(複数の網膜専門家集団による統一見解)。 右上は、モデルが予測したスコア(N=DRではない、Mi=軽度のDR,Mo=中程度のDR)の実例です。右下は、モデルによる支援なしで単独の医師が下した診断(Unassisted)とモデルによる支援を受けた医師による診断(Grades Only)です。(訳注:要はMoが正解だけれども、右上の人工知能オンリーの診断でも右下の単独の医師が下した診断でも誤認が入ってきてしまっているけれども、医師+人工は間違えなかったと言う事です)
医学および眼科の専門家によって非常に注目された研究として、私達は、網膜像から心血管リスクを評価することができる機械学習モデルに関する研究を発表しました。これは、臨床医が彼らの患者の健康状態をよりよく理解する事を助ける新しい非侵襲性バイオマーカーとして有望な兆候を示しています。
私たちは今年も病理学に焦点を合わせ続け、MLを用いた前立腺癌の悪性度の評価、ディープラーニングによる転移性乳癌の検出、リアルタイムで顕微鏡の視野にコンピュータビジョンモデルから得られた視覚情報を重ね合わせることによって病理学者や他の科学者を助けることができる拡張現実顕微鏡のプロトタイプを開発しました。
過去4年間、我々は適切な臨床予測をするためにEHR(電子カルテ)にディープラーニングを適用する重要な研究努力をしてきました。2018年に、シカゴ大学医学部、UCSFおよびスタンフォード医学と共同で、私たちはNature Digital Medicine誌に論文を発表し、匿名の電子医療記録に対してMLモデルが行った診断が、現在の臨床的なベストプラクティスよりも様々な臨床的課題に対して有意に高い精度の予測を行う方法を示しました。
この作業の一環として、病院や組織によって異なるタスクや書式を基礎とするEHRデータセットに対しても、これらのモデルを作成することを非常に簡単にするためのツールを開発しました。
私たちはこの研究でFHIR(Fast Healthcare Interoperability Resources)標準に準拠するオープンソースソフトウェアを開発しました。これは医療データをより簡単に、より標準化するために役立ちます。(GitHubレポジトリを参照してください)
また、ディープラーニングベースのゲノム解析ツールであるDeepVariantの精度、速度、および有用性を向上させました。チームはパートナーと共に前進し、最近Nature Biotechnologyに査読論文を発表しました。
歴史的に収集されたデータにMLを適用する際には、過去に人間的および構造的な偏りを経験した母集団、およびそれらの偏りがデータ内でどのように体系化されてきたかを理解することが重要です。 機械学習は、偏りを検出して対処し、全ての人が健康になるように公平性を積極的に向上させる機会を提供します。
(2018年のGoogleの研究成果を振り返って(4/6)からの続きです)
(2018年のGoogleの研究成果を振り返って(6/6)に続きます)
3.2018年のGoogleの研究成果を振り返って(5/6)関連リンク
1)ai.googleblog.com
Looking Back at Google’s Research Efforts in 2018



コメント