1.LYNA:ディープラーニングを用いて転移性乳癌を検出する試みまとめ
・LYNAはディープラーニングで画像から乳癌の転移を見つける試み
・LYNAと病理学者が共に働く事により高いパフォーマンスを示せた
・実際の治療現場で使われるようになるまではまだ課題がある
2.LYNAとは?
以下、ai.googleblog.comより「Applying Deep Learning to Metastatic Breast Cancer Detection」の意訳です。
病理学者が顕微鏡を使って患者の腫瘍を診断する事は、癌診断で一番重視されている診察方法であり、予後と治療の決定に大きな影響を与えます。
この病理学的診断の重要な、しかし厄介な側面の1つは、主要患部から近隣のリンパ節に拡がった(転移した)癌を検出することです。癌の転移の検出は、ほとんどの癌に関連し広く使用されているTNM癌ステージング分類を決定する際に使われる基礎的な部分です。特に乳癌では結節(nodal)転移の有無が、放射線療法、化学療法、および追加のリンパ節の外科的除去の必要性など、追加治療の決定に大きな影響を及ぼします。
したがって、結節転移を正確に素早く診断する事は臨床治療において非常に重要です。しかし、研究では、転移性リンパ節のステージ分類の約4分の1が二度目の病理学的診断レビューの際に変更される事がわかっています。また、個々のスライド上で癌の小さい転移を検出する事は、時間的制約を抱えながら実施すると精度が38%低くなり得ることも示されています。
昨年、私達はディープラーニングを用いて診断結果の正確性をアシストするLYNA(リンパ ノード アシスタント)を説明し、2016 ISBI Camelyon Challengeでは研究者が転移癌を検出するためのコンピュータアルゴリズムを開発するために乳癌患者のリンパ節のギガピクセルサイズの病理画像スライドを提供しました。
LYNAはこれまで報告されていたよりもはるかに高い癌検出率(Liu等による2017の発表)を達成しましたが、正確なアルゴリズムと言うだけでは病理学者のワークフローを改善したり、乳がん患者の転帰を改善するには不十分でした。
患者の安全のためには、これらのアルゴリズムは、その強みと弱みを明確にするために様々な設定でテストされる必要があります。さらに、これらのアルゴリズムを使用する事による病理学者にとっての利益は、これまで検討されておらず、アルゴリズムが効率または診断精度を実際に向上させるか否かを判断するために評価されなければなりません。
論文「Artificial Intelligence Based Breast Cancer Nodal Metastasis Detection: Insights into the Black Box for Pathologists」(Liu等による2018の発表)は、 Archives of Pathology and Laboratory Medicine誌に掲載され、論文「Impact of Deep Learning Assistance on the Histopathologic Review of Lymph Nodes for Metastatic Breast Cancer」(Steiner, MacDonald, Liu等による2018の発表)は、American Journal of Surgical Pathology誌に掲載されました。私達はLYNAに基づく病理学者支援ツールのコンセプトをプレゼンし、これらの実証結果を調査しました。
最初の論文では、Camelyon Challengeのデータセットと、Naval Medical Center San Diegoの共著者によって提供された異なるデータセットを用いて、癌画像のスライドの識別をアルゴリズムに行わせました。この追加のデータセットは、異なる処理を行う異なる研究所からの病理サンプルで構成されていたため、日常的な臨床診療で見られるスライドや人工的な処置の多様性に対する対応力を改善できました。LYNAは画像のばらつきや患部に人工的な処置がされている部分(artifacts)があっても問題なく識別できる事を示し、追加の開発なしで両方のデータセットで同様の性能を達成しました。
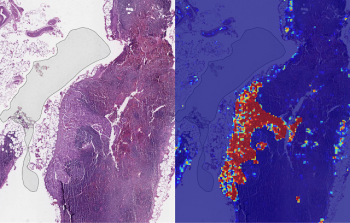
左図:リンパ節を含むスライドのサンプルビューで、複数の人工物があります。左の暗いゾーンは気泡、白い筋は切断面、一部の領域の赤色は出血(血液を含む)、組織は壊死しています。処置が貧弱でした。右図:LYNAは、中央の腫瘍領域(赤色)を識別し、周囲の人工物を含む領域を非腫瘍(青色)として正しく分類しています。
両方のデータセットにおいて、LYNAは癌のないスライド画像から転移性癌を有するスライドを正確に区別することができました。さらに、LYNAは、各スライド内の癌および他の疑わしい領域の位置を正確に特定することができ、そのいくつかは小さすぎて病理学者が一貫して検出する事は難しいレベルでした。このように、私たちは、LYNAの潜在的な利点の1つは、病理学者が最終的な診断を検討し決定することについてのこれらの懸念事項を強調することであると推論しました。
我々の2番目の論文では、6人の病院認定病理学者が、LYNAの助けを借りずに、転移性乳がんのリンパ節を検査する模擬診断作業を行いました。LYNAを使用することで、病理学者の自己診断による難しさが主観的に「容易」になり、平均スライドレビュー時間が半分になり、 1スライドにつき2分かかっていたところが1分で済むようになりました。

左図:リンパ節を含むスライドのサンプルビューで、転移性の乳房腫瘍が漸進的に拡大します。右図:同じ画像で、アルゴリズムの「支援」(LYNA LYmph Node Assistant)によりシアン色での腫瘍を目立たせた画像。
この実験結果は、LYNAのようなアシストテクノロジーは、病理画像を繰り返し判定するような作業の負担を軽減し、病理学者が他のより困難な臨床および診断作業に集中するために、より多くの時間と労力を費やすことを可能にする潜在能力がある事を示しています。
診断精度に関して、この研究の病理学者はLYNAが発見した微小な転移をより確実に検出することができ、見逃した微小転移の割合を減少させました。勇気づけられる事に、LYNAの支援を受けた病理学者は、支援を受けていない病理学者またはLYNAアルゴリズム自体よりも正確であり、人々とアルゴリズムが共に働く事は、それぞれが単独で働くより効果的に機能することを示唆しています。
これらの研究により、我々は乳癌TNMステージング診断をサポートするLYNAアルゴリズムの堅牢性を実証し、実証実験によりその影響を評価するところまで進展しました。勇気づけられる結果ではありますが、これらのタイプの技術を実験室から医師や患者を助ける実際の医療現場のベッドまでの旅させる事は、まだまだ長い道のりです。
これらの研究には、まだ重大な制限があります。限られたデータセットサイズや、通常の完全な臨床診断に用いられる複数のスライドではなく、全ての患者で単一のリンパ節スライドのみを調べる模擬診断ワークフローを用いた事など。
更に実際の臨床ワークフローと患者の転帰に及ぼすLYNAの影響を評価するためには、今後、もっと沢山の作業が必要になります。しかしながら、私達は慎重に検証されたディープラーニングテクノロジーと上手に設計された臨床ツールが世界中の病理学的診断の正確さと可用性の両方を改善するのに役に立つだろうと楽観的です。
3.LYNA:ディープラーニングを用いて転移性乳癌を検出する試み感想
少し前にJeff Deanのツイッターに奥さんがステージ4の癌なんだ、貴方が最後の希望なんだ助けてほしい、と訴えていたお爺さんを見かけたのですが、現在の人工知能は最先端であっても、この記事のように診断を補佐するくらいしかできないので、心が痛みました。
4.LYNA:ディープラーニングを用いて転移性乳癌を検出する試み関連リンク
1)ai.googleblog.com
Applying Deep Learning to Metastatic Breast Cancer Detection
2)www.archivesofpathology.org
Artificial Intelligence–Based Breast Cancer Nodal Metastasis Detection
3)insights.ovid.com
Impact of Deep Learning Assistance on the Histopathologic Review of Lymph Nodes for Metastatic Breast Cancer